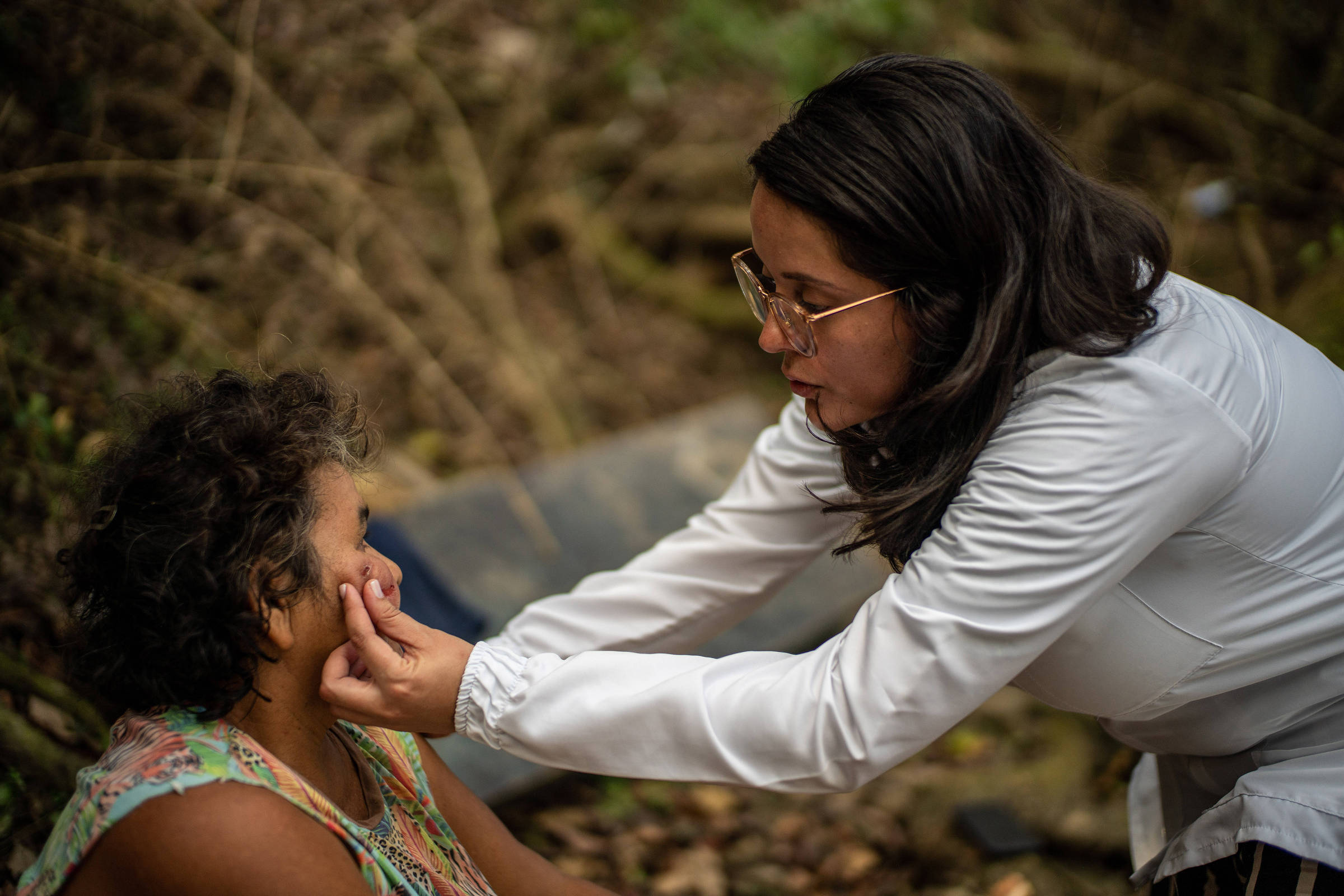
Há três anos, Jesús Tilano, 85, foi a um hospital em uma região de floresta densa, na Colômbia, com grandes lesões abertas no nariz, no braço direito e na mão esquerda. Recebu o diagnóstico de leishmaniose, doença parasitária transmitida pela picada de um flebotomíneo fêmea –também conhecido como mosquito-palha–, que comumente acomete pessoas pobres que trabalham no campo ou em áreas florestais de países em desenvolvimento.
Para o tratamento de Tilano, foi prescrito um medicamento que requer três injeções diárias durante 20 dias –cada uma delas muito dolorosa. Para conseguir se tratar, ele precisou fazer repetidas e caras viagens de ônibus à cidade. Depois, os rins começaram a falhar –efeito colateral comum do medicamento, assim como insuficiência cardíaca e problemas hepáticos.
“O tratamento me deixou pior do que eu estava antes”, resume ele.
A leishmaniose é uma doença difícil e envolve tratamentos penosos que não apresentaram praticamente nenhuma evolução em quase um século. O medicamento que Tilano tomou foi usado pela primeira vez há 70 anos, e todos os procedimentos combinam sintomas dolorosos, toxicidade, custo alto e aplicação difícil, exigindo internação hospitalar ou idas diárias a um consultório durante um mês.
Segundo os especialistas, entre as “doenças tropicais negligenciadas”, a leishmaniose, que foi identificada há 120 anos pela primeira vez, já ganhou uma distinção no que diz respeito à “falta de progresso” para ajudar os dois milhões de pessoas que a contraem anualmente.
Mas esse cenário está, finalmente, começando a mudar: quando o neto de Tilano, Andrés Tilano, 14, contraiu a doença no ano passado, foi tratado em uma clínica em Medellín, com uma terapia experimental que curou a infecção no período de alguns dias.
O tratamento que ele recebeu é um dos vários que estão sendo desenvolvidos pelo Programa de Estudo e Controle de Doenças Tropicais (Pecet, em espanhol), um pequeno instituto de pesquisa sediado na Universidade de Antioquia, em Medellín. Como parte do esforço de buscar novas abordagens para a leishmaniose, o programa se associou à iniciativa Medicamentos para Doenças Negligenciadas (DNDi, em inglês), uma organização de pesquisa e desenvolvimento sem fins lucrativos sediada em Genebra.
Todos os tratamentos experimentais que os pesquisadores estão avaliando são muito menos tóxicos, mais simples e mais baratos do que os atuais. Mas um grande obstáculo ainda impede que eles cheguem às milhões de pessoas que precisam deles: nenhum dos novos procedimentos foi testado em um ensaio em larga escala, nem aprovado pelo órgão regulador de medicamentos da Colômbia, nem adotado pelas diretrizes nacionais de tratamento da doença. Quando uma medicação é fabricada por uma empresa farmacêutica, ela é submetida a um processo regulatório que é caro e demorado.
Mas não se ganha dinheiro com um medicamento para uma doença que acomete predominantemente a população pobre, e os institutos acadêmicos ou de saúde pública raramente têm recursos para levá-lo até o fim do processo, explica Marcela Vieira, advogada brasileira da área de propriedade intelectual, especializada em acesso e elaboração de medicamentos e pesquisadora do Centro de Saúde Global do Instituto de Pós-Graduação em Estudos Internacionais e de Desenvolvimento, em Genebra.
O sistema global de desenvolvimento de medicamentos sempre favoreceu empresas do setor privado que podem financiar experimentos voltados para doenças que afetam pessoas que têm dinheiro para pagar por tratamentos. Cada vez mais, novas pesquisas sobre enfermidades, como a leishmaniose, vêm do setor público e de instituições acadêmicas de países de renda média, especialmente do Brasil, da África do Sul, da Índia, de Cuba e da China, diz Vieira.
A pandemia de Covid, durante a qual nações menos favorecidas economicamente foram relegadas ao fim da fila para vacinas e tratamentos, ajudou a impulsionar novos investimentos na construção de capacidade de desenvolvimento e produção de medicamentos. “Precisamos fazer isso, porque ninguém vai fazer por nós”, afirma Juliana Quintero, especialista em leishmaniose e pesquisadora do Pecet.
Os pesquisadores de leishmaniose se inspiraram nos povos indígenas da região: um dos medicamentos que está sendo testado, um gel aplicado às lesões, é derivado de uma planta que os indígenas usam para combater o parasita. O tratamento experimental que curou Andrés Tilano, chamado de termoterapia, assemelha-se à cura tradicional indígena de queimar as lesões. Em sua clínica, Quintero usou um dispositivo portátil que emitia calor a uma temperatura de 50ºC, matando o parasita nas camadas internas da pele.
Hoje, ela prescreve dois tratamentos que seu instituto desenvolveu e os fornece aos pacientes sob um “programa de uso compassivo” para medicamentos que ainda não foram aprovados ou registrados pelo governo colombiano.
A DNDi, organização sem fins lucrativos, examinou mais de dois milhões e meio de compostos –primeiro passo padrão no desenvolvimento de medicamentos– para chegar a cinco estruturas químicas que pareciam, em testes de laboratório iniciais, ser efetivas contra o parasita que causa a leishmaniose. Mas, das cinco, só uma ou duas avançarão para ensaios clínicos maiores, declara Jadel Kratz, responsável pelo trabalho de descoberta de medicamentos da organização na América Latina.
Ele pontua que a descoberta inicial e os estudos pré-clínicos custam de US$ 10 milhões a US$ 20 milhões, enquanto os primeiros ensaios clínicos pequenos, voltados para segurança e sinais de eficácia, podem custar mais de US$ 6 milhões. A última fase, que consiste em um grande ensaio em pacientes para testar se o medicamento funciona, custa, no mínimo, US$ 20 milhões –muito mais do que equipes de pesquisa públicas e acadêmicas podem financiar.
“É um enorme risco para a pesquisa local se só as corporações multinacionais puderem fazer esse trabalho”, diz Iván Darío Vélez-Bernal, que se aposentou recentemente como diretor do Pecet.
Mas o foco da DNDi na leishmaniose e o trabalho de pesquisadores em uma rede que inclui a Índia, a Colômbia e o Brasil estão começando a dar resultados. Hoje, existem cinco medicamentos em fase 1 de testes e outro na Fase 2, o que é inédito na história da doença. Contudo, não está claro quando, ou como, as medicações chegarão às próximas fases do processo. Medicamentos provenientes de instituições públicas tendem a ficar estagnados sem um defensor ativo, observa Vieira.